Dwutlenek chloru
Dwutlenek chloru ClO2 – nieorganiczny związek chemiczny, tlenek chloru na IV stopniu utlenienia. Jest silnym utleniaczem o dużej trwałości. W stanie czystym lub w wysokich stężeniach rozkłada się wybuchowo na pierwiastki pod wpływem światła, sprężenia lub po niewielkim ogrzaniu.
- Właściwości fizyczne
- Rozpuszczalność i stabilność
- Właściwości dezynfekcyjne
- Dwutlenek chloru – Legionella
- Dwutlenek chloru – bakteria E.coli
- Trwałość dwutlenku chloru
- Dawka i zapotrzebowanie
- Dwutlenek chloru w uzdatnianiu wody
- Reaktywność z żelazem i manganem
- Dezynfekcja wody powierzchniowej
- Dezynfekcja końcowa wody
- Dezynfekcja zbiorników
- Dezynfekcja ścieków
- Dezynfekcja ścieków szpitalnych
- Dezynfekcja w przemyśle spożywczym
- Obróbka wody chłodzącej, biofilm
- Wytwarzanie dwutlenku chloru
- Generatory dwutlenku chloru
- Kwas solny
- Chloryn sodu
- Bezpieczeństwo i przechowywanie
- Toksyczność dwutlenku chloru
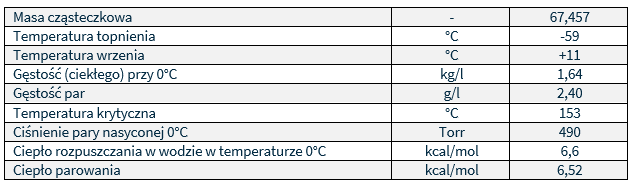
W temperaturze pokojowej dwutlenek chloru (ClO2) jest gazem gęstszym od powietrza o barwie żółto-szarej, dobrze rozpuszczalnym w wodzie.
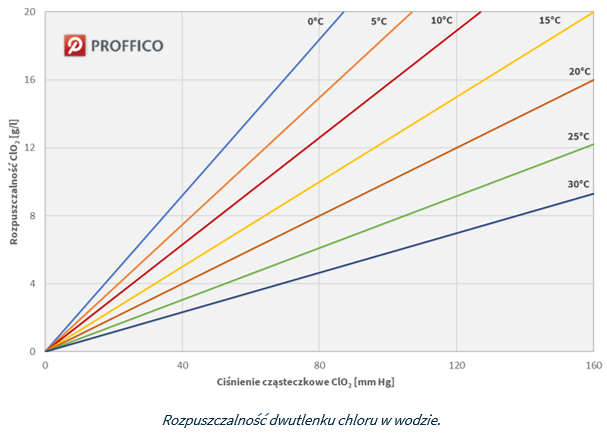
Dwutlenek chloru (ClO2) jest wysoce rozpuszczalny w wodzie, bardziej niż chlor czy ozon. Rozpuszczalność gazu jest wyrażona przez stężenie gazu rozpuszczonego w stanie równowagi tzn. pomiędzy jego stanem gazowym a rozpuszczonym. Wykresy poniżej przedstawiają wartości stężenia CIO2 przy różnych temperaturach i ciśnieniach cząstkowych. Na rozpuszczalność CIO2 nie ma wpływu potencjalna obecność chloru w wodzie. W przedziale wartości pH charakterystycznych dla wody pitnej (tj. 6÷8) dwutlenek chloru nie ulega hydrolizie, lecz pozostaje w roztworze jako gaz rozpuszczony.
Obecność jonów podchlorynowych (CIO) powoduje, że dwutlenek chloru ulega rozkładowi przy umiarkowanie zasadowym pH środowiska. Obecność jonów chlorynowych (CIO2–) ma niewielki wpływ, jednak w połączeniu z podchlorynem przyspiesza utratę dwutlenku chloru. Z praktycznego punktu widzenia, obserwacje te są ważne, ponieważ stabilność wodnych roztworów dwutlenku chloru jest związana z jego czystością. Ponadto, rozkład dwutlenku chloru w roztworze wodnym jest intensyfikowany przez światło i w tym przypadku produktami rozkładu są głównie jony chlorkowe (CI–) i jony chloranowe (CIO3–). Światło niebieskie i UV jest skuteczne w fotodekompozycji dwutlenku chloru, gdzie szybkość reakcji jest uzależniona od intensywności światła. Dlatego, aby zachować wymaganą stabilność roztworu, wodny dwutlenku chloru musi być przechowywany w zamkniętych pojemnikach, w niskiej temperaturze i z dala od światła. Umiarkowane zakwaszenie (pH = 6) może ułatwić stabilizację i zapobiec rozkładowi dwutlenku chloru.
Rozpuszczalność i stabilność w roztworach wodnych – pobierz pdf.
Dwutlenek chloru ma doskonałe właściwości bakteriobójcze, wirusobójcze, sporobójcze i glonobójcze, dlatego też stosowany jest masowo do dezynfekcji wody. W przeciwieństwie do chloru czy podchlorynu sodu właściwości utleniające i dezynfekujące dwutlenku chloru pozostają praktycznie niezmienione w szerokim zakresie pH (od 4 do 10).
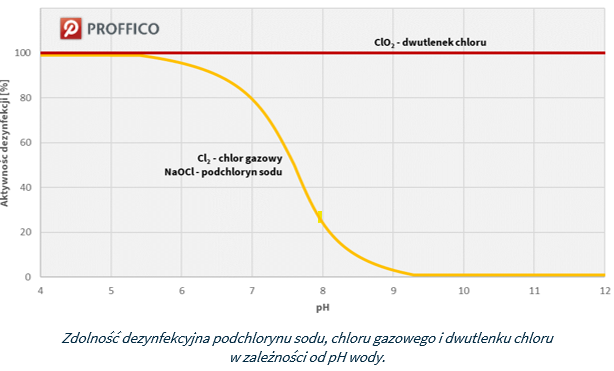
Ocena skuteczności środka dezynfekującego opiera się zazwyczaj na pojęciu „stężenie i czas trwania” [Sxt]. Wskaźnik ten odnosi się do stężenia dozowanego środka dezynfekującego i czasu kontaktu potrzebnego do zniszczenia wybranych szczepów bakterii czy wirusów przy użyciu danego dezynfektanta. Zależność między stężeniem [S], a czasem kontaktu [t], jest wyrażona następującym równaniem empirycznym:
k = Sn • t
gdzie:
S – jest stężeniem środka dezynfekującego,
n – jest współczynnikiem rozcieńczenia,
t – jest to czas kontaktu wymagany do osiągnięcia określonego % dezaktywacji,
k – jest specyficzną stałą dla każdej populacji drobnoustrojów.
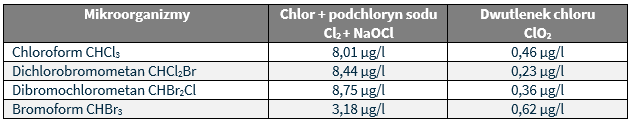
Na podstawie tego wskaźnika i działając w określonych warunkach i na wybranych mikroorganizmach, możliwe jest porównanie skuteczności różnych środków dezynfekcyjnych. Dlatego im niższa wartość tego wskaźnika w odniesieniu do określonej grupy bakterii tym dany środek dezynfekcyjny jest bardziej aktywny. W tabeli poniżej podano wartości wskaźnika [Sxt] w odniesieniu do skuteczności niektórych środków dezynfekcyjnych w unieszkodliwianiu 99% różnych mikroorganizmów.
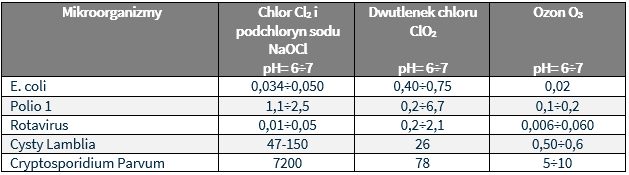
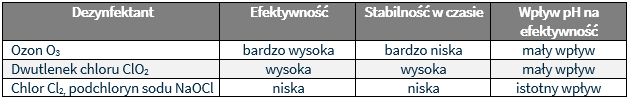
Wydajność biobójcza chloru i podchlorynu sodu szybko maleje, przechodząc od pH 7, w którym dominującą postacią jest kwas chlorowodorowy (HCIO) do pH 9, w którym dominującą postacią jest jon podchlorynu (CIO–). W tym samym przedziale pH wydajność biobójcza dwutlenku chloru utrzymuje się nadal na stałym poziomie. Dzięki swojej stabilności i trwałości w czasie dwutlenek chloru jest szczególnie stosowany przy dezynfekcji końcowej uzdatnianej wody tj. przed jej wprowadzeniem do zbiorników retencyjnych lub sieci. Głównym walorem w tym przypadku jest najdłuższy czas działania tego środka pozwalający na dezynfekcję końcówek sieci oraz niepogorszanie smaku i zapachu dezynfekowanej wody. Taka dezynfekcja może być osiągnięta dzięki sekwencyjnemu działaniu dwutlenku chloru (skuteczny środek bakteriobójczy) i chlorynu (bakteriostatyczny i lekko biobójczy). W tabeli poniżej przedstawiono skuteczność biobójczą, stabilność oraz wpływ pH na skuteczność niektórych środków dezynfekcyjnych.
Mechanizm, za pomocą którego dwutlenek chloru inaktywuje mikroorganizmy, nie jest jeszcze w pełni poznany, ale był i jest celem dwóch rodzajów badań. Z jednej strony badane są reakcje chemiczne CIO2 z molekularnymi składnikami komórek mikroorganizmów, a z drugiej strony badany jest wpływ CIO2 na ich funkcje fizjologiczne. Badania wykazały szybką reaktywność CIO2 z niektórymi aminokwasami (takimi jak cysteina, tryptofan i tyrozyna), ale nie z kwasem rybonukleinowym (RNA) w wirusach. Wnioski wynikające z tych badań są takie, że inaktywacja wirusów przez CIO2 jest spowodowana zmianą zawartości białek w kapsydach wirusowych. Inne badania wskazują jednak na reakcję CIO2 z RNA Poliowirusa w takim stopniu, aby uszkodzić syntezę samego RNA. Inni badacze natomiast stwierdzili, że CIO2 jest reaktywny z kwasami tłuszczowymi w błonie cytoplazmatycznej. Badania nie wyjaśniły jeszcze, czy pierwotne działanie CIO2 ma miejsce na poziomie struktur obwodowych (błony komórkowe), czy też struktur wewnętrznych (jądro, mitochondria). Uzasadnione jest jednak przypuszczenie, że oba te działania przyczyniają się do inaktywacji mikroorganizmów. W każdym razie, działanie na poziomie struktur peryferyjnych (zmiany białek i lipidów błony komórkowej) spowodowałoby wzrost przepuszczalności samej błony, natomiast działanie na poziomie struktur wewnętrznych prowadziłoby do zmian w syntezie proteinowej i/lub w aktywności oddechowej. W każdym razie, wymienione powyżej działania ostatecznie prowadzą do śmierci komórki.
Dwutlenek chloru jest jedynym dezynfekantem, który skutecznie eliminuje bakterie Legionelli. Legionella może występować wszędzie, ale największe jej skupiska stwierdza się w instalacjach wody ciepłej w budynkach użyteczności publicznej (m.in. w szpitalach, domach opieki, hotelach, itp.). Ponadto 90% bakterii Legionella znajduje się w śluzie biofilmu, a tylko 10% w wodzie. Biofilm chroni mikroorganizmy przed działaniem substancji dezynfekcyjnych. W celu całkowitej eliminacji zarazków Legionella należy usunąć i zapobiegać powstawaniu biofilmu pokrywającego rurociągi oraz urządzenia technologiczne, a z tym świetnie radzi sobie właśnie dwutlenek chloru. Ponadto stałe dozowanie odpowiedniej ilości dwutlenku chloru do wody zabezpiecza instalację wodociągowe przed rozwojem bakterii Legionella i jej wtórnym skażeniem.
Właściwości dezynfekcyjne dwutlenku chloru – Legionella – pobierz pdf.
Poniższy wykres ukazuje wpływ niektórych środków dezynfekujących na niszczenie 99% szczepów E. coli przy temperaturze wody na poziomie 150C. Z wykresów wynika, że chlor i podchloryn sodu wydają się być bardziej skuteczne niż dwutlenek chloru w inaktywacji E. coli ale odnosi się to jedynie do przypadku, gdy dezynfekowana woda ma p niższe niż 7. Przy pH powyżej 7, gdy chlor i podchloryn sodu występują w postaci jonu podchlorynowego (ClO–) i chloramin (NHCl2, NH2Cl), zdolność dezynfekcyjna dwutlenku chloru jest wyższa.
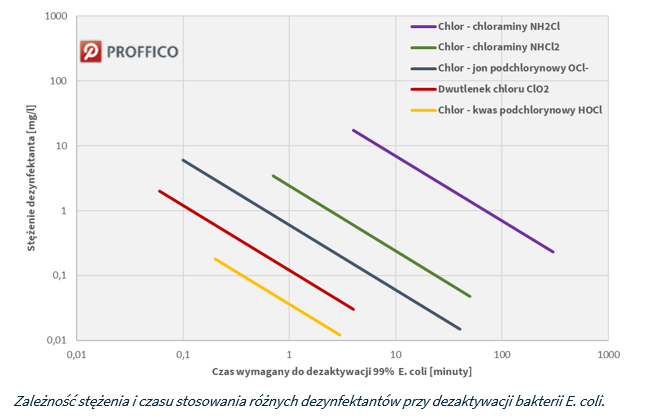
Właściwości dezynfekcyjne dwutlenku chloru – bakteria E.coli – pobierz pdf.
Ponieważ dwutlenek chloru jest stosunkowo nietrwałym gazem, który staje się wybuchowy, gdy jego stężenie w powietrzu jest większe niż 10% objętości, gaz ten nie może być sprężany i skraplany a zatem musi być wytwarzany na miejscu dozowania „in situ” i następnie rozpuszczany w wodzie.
Roztwory dwutlenku chloru przy stężeniu 30 g/l lub większym są niebezpieczne. Roztwory rozcieńczone do 3 g ClO2/l są w pełni bezpieczne i stabilne dlatego mogą być stosowane w procesie dezynfekcji. Czynniki, które mogą powodować zmianę stabilności tych roztworów to pH, obecne zanieczyszczenia, ciepło i światło.
Przy każdym zastosowaniu dwutlenku chloru, jak również przy zabiegach z użyciem chloru lub podchlorynu sodu ważne jest, aby przed rozpoczęciem dozowania określić „zapotrzebowanie wody na dany środek dezynfekcyjny”.
Zapotrzebowanie na dwutlenek chloru oznacza nic innego jak ilość dwutlenku chloru, który reaguje z badaną wodą w określonym czasie (od 5 do 60 minut, w zależności od czasu kontaktu w instalacji). Powszechnie wartość ta jest określana jako tzw. „punkt przełamania” i stanowi obszar odniesienia do dalszych zastosowań dwutlenku chloru, ponieważ jest ona w pewnym sensie oceną jakości dezynfekowanej wody.
W odniesieniu do punktu dozowania rozróżnia się dawkowania niższe, równe i nieco wyższe niż samo zapotrzebowanie. Dozowanie niższe stosuje się dla ścieków, gdzie 20-30% zapotrzebowania jest zwykle wystarczające do osiągnięcia wymaganego poziomu bakteriologicznego. Dozowanie równe punktowi przełamania stosuje się przy uzdatnianiu wody pitnej w trakcie utleniania wstępnego. Dozowanie z nadwyżką stosuje się przy dezynfekcji końcowej wody pitnej.
Należy pamiętać, że zapotrzebowanie to odnosi się do całkowitego zapotrzebowania wody przeznaczonej do uzdatniania na dwutlenek chloru i w związku z tym obejmuje ilość CIO2 zużytego w reakcji z obecnymi mikroorganizmami oraz ilość CIO2 zużytego w reakcji z wcześniejszymi chemikaliami. Z tego samego powodu, w celu osiągnięcia prawidłowego stosowania CIO2 i uzyskania założonego celu, konieczne jest przeprowadzenie innych analiz uzupełniających (na przykład niektórych analiz mikrobiologicznych lub rzeczywistych testów przeprowadzanych bezpośrednio na danym obiekcie).
Dwutlenek chloru może być stosowany w uzdatnianiu wody pitnej jako środek dezynfekujący, albo jako utleniacz. Jako środek dezynfekujący może być stosowany zarówno w fazie wstępnej, jak i w fazie końcowej.
W utlenianiu wstępnym przy wodach powierzchniowych dwutlenek chloru jest wykorzystywany do zapobiegania rozwojowi bakterii i glonów w kolejnych fazach uzdatniania. Zastosowanie dwutlenku chloru w tej fazie, w przeciwieństwie do chloru czy podchlorynu sodu ma tę zaletę, że znacznie ogranicza powstawanie chlorowcowanych związków organicznych w tym trójhalometanów (THM). Możliwość tworzenia się THM-ów jest wyższa w przypadku wód powierzchniowych zawierających wysokie poziomy prekursorów organicznych. Ponadto w fazie utleniania wstępnego, dwutlenek chloru utlenia substancje koloidalne poprawiając tym samym proces koagulacji redukujący mętność wody. Działanie dwutlenku chloru w procesie utleniania wstępnego jest związane przede wszystkim z materią organiczną, obecną zarówno w formie rozpuszczonej, jak i koloidalnej. Jednakże w przypadku dwutlenku chloru nie ma znaczenia pH i temperatura, która może silnie wpływać na inne procesy utleniania wstępnego (klasycznym przypadkiem jest podchloryn sodu). Ewentualne pozostałości dwutlenku chloru mogą być łatwo usunięte przez następujące po sobie przejścia przez filtry z granulowanym węglem aktywnym.
Dwutlenek chloru jako utleniacz w uzdatnianiu wody jest używany przy: usuwanie żelaza i manganu z wody, zmniejszanie mętności i barwy wody, usuwanie zapachów i smaków, kontroli wzrostu glonów oraz usuwanie niektórych pestycydów z wody. Mechanizm działania dwutlenku chloru w tym zakresie przedstawi się następująco:
- żelazo i mangan są obecne w wodzie w formie zredukowanej lub w kompleksach z substancjami organicznymi (w szczególności z kwasem humusowym i fulwowym) i są utleniane do wodorotlenków, które poprzez fizyczne wytrącanie są zatrzymywane na złożach filtracyjnych. W tym przypadku dwutlenek chloru jest znacząco skuteczniejszy niż chlor czy podchloryn sodu, ponieważ przy pH > 7 szybkość reakcji dwutlenku chloru w odniesieniu do manganu jest bardzo szybka. Ponadto, w przeciwieństwie do chloru i podchlorynu sodu, reakcja utleniania nie wiąże się ze znacznym obniżeniem alkaliczności wody i wynikającą z tego zmianą bilansu wapniowo węglanowego w uzdatnianej wodzie.
- mętność wody jest związana z obecnością w zawiesinie cząstek koloidalnych, których eliminacja wymaga podania koagulantów. W tej fazie uzdatniania działanie dwutlenku chloru, jest pomocne poprzez utleniające jego działanie na substancje pokrywające koloidy które utrzymują je w zawiesinie a po zadozowaniu dwutlenku chloru zachodzi proces wspomagania tworzenia się kłaczków.
- obecność zapachów i smaków w wodzie jest spowodowana licznymi związkami: metabolitami organizmów (glonów, aktynomiocytów itp.) obecnych w wodach powierzchniowych; fenolami, pochodzącymi z zanieczyszczeń przemysłowych lub powstałymi w wyniku rozkładu glonów, lub występującymi z chloraminami powstałymi w przypadkach, gdy woda została wstępnie utleniona chlorem czy podchlorynem sodu; chlorkami i bromkami obecnymi w wodach gruntowych zanieczyszczonych np. wodą morską; węglowodorami.
- utleniające, bakteriobójcze, grzybobójcze i glonobójcze działanie CIO2 sprawia, że jest on wykorzystywany do poprawy właściwości organoleptycznych wody bez powstawania chlorofenoli i chloramin. Jednak należy pamiętać jest on niereaktywny z niektórymi węglowodorami co może spowodować, że będzie on nieskuteczny w usuwaniu niektórych zapachów.
- obecność glonów nadaje wodzie nieprzyjemny zapach, smak i barwę, utrudnia usuwanie mętności i może blokować lub zanieczyszczać system dystrybucji lub filtry piaskowe. Dwutlenek chloru jest skuteczny i w tym przypadku, ponieważ posiada on zdolność do atakowania piroliferycznego pierścieni łańcuchowych chlorofilu. Dlatego przy stosowaniu dwutlenku chloru w tym celu stosuje się dawkę w zakresie 0,5 ÷ 1,0 mg/l przy dodawaniu do wody przechowywanej w zbiorniku (najlepiej w godzinach nocnych, aby uniknąć jego degradacji pod wpływem działania światła słonecznego).
- pestycydy, które mogą być usuwane za pomocą CIO2 to DMDT (dimetoksodichlor) i aldryna. Herbicydy, takie jak parakwat i dikwat, są eliminowane w ciągu kilku minut, jednakże przy pH powyżej 8. W celu wstępnego utlenienia i redukcji zanieczyszczeń organicznych, wymagane dawki wynoszą od 0,5 do 2,0 mg/l, przy czym czas kontaktu w zależności od jakości wody zwykle wynosi od 15 do 30 minut
Jak wskazują potencjały redox Fe3+ / Fe2+ i Mn4+ / Mn2+, jony Fe2+ i Mn4+ są utleniane przez dwutlenek chloru z utworzeniem odpowiednio wodorotlenku żelaza i dwutlenku manganu, które będąc słabo rozpuszczalne lub wytrącone będą się osadzały na stałych elementach danego systemu.
Fe3+ + e– ↔ Fe2+ E0 = 0,77 V
Mn3+ + 2e– ↔ Mn2+ E0 = 0,37 V
Reakcje utleniania-redukcji przy pH 7 są następujące:
ClO2 + Fe2+ → Fe3+ + ClO2–
Fe3+ + 3 OH– → Fe (OH)3
2 ClO2 + Mn2+ + 2H2O → 2 ClO2– + MnO2 + 4 H+
Przy pH większym od 7 następuje pełna redukcja do Cl–
Teoretyczne zużycie ClO2 wynosi:
1,2 mg ClO2 na mg Fe2+
1,45 mg ClO2 na mg Mn2+
Zaletą dwutlenku chloru jest to, że stopień jego utleniania jest wyższy niż w przypadku chloru czy podchlorynu sodu. Zdolność dwutlenku chloru do utleniania żelaza i manganu, a tym samym pozyskiwania ich z wody poprzez wytrącanie, jest wykorzystywana w szczególności w uzdatnianiu wody przeznaczonej do spożycia przez ludzi.
Reaktywność dwutlenku chloru z żelazem i manganem – pobierz pdf.
Na stacji uzdatniania wody, która ujmuję wodę powierzchniową pochodzącą z górskiej rzeki, przeprowadzono testy mające na celu ocenę możliwości zastąpienia obecnego sposobu dezynfekcji podchlorynem sodu na rzecz dwutlenku chloru. Obecna dezynfekcja przeprowadzana jest zarówno w procesie utleniania wstępnego jak i przy dezynfekcji końcowej.
Problemy związane z dezynfekcją przy użyciu podchlorynu sodu spowodowane były przede wszystkim nadmiernym tworzeniem się chlorowanych związków organicznych, które przekroczyły dopuszczalne limity 50 µg AOX/I, częściowo z powodu wstępnego utleniania (dawka 3,0 mgCl2/l), a częściowo z powodu dezynfekcji końcowej (dawka 1,2 mgCl2 /l).
Właściwości chemiczne i mikrobiologiczne wody na wejściu do stacji przedstawiają się następująco:
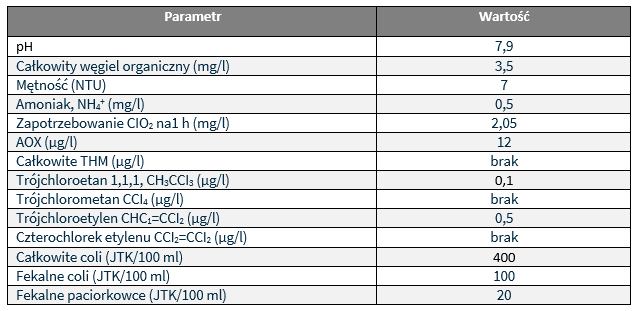
Właściwości chemiczne i mikrobiologiczne wody poddanej działaniu podchlorynu sodu w utlenianiu wstępnym i dezynfekcji końcowej:
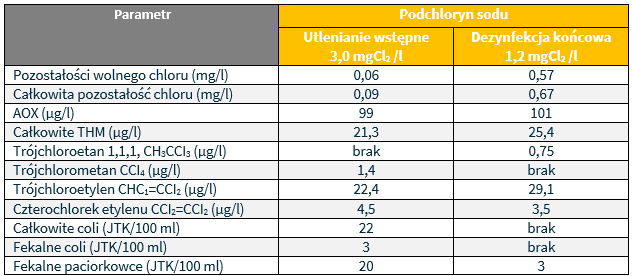
Dezynfekcję wody dwutlenkiem chloru przeprowadzono na wodzie surowej z godzinnym czasem kontaktu i w dawkach wynoszących odpowiednio 2,05 i 1,74 i 1,43 i 1,02 mg/l odpowiadających 100, 85, 70 i 50% zapotrzebowania wody na CIO2. Wyniki przedstawiono w poniższej:
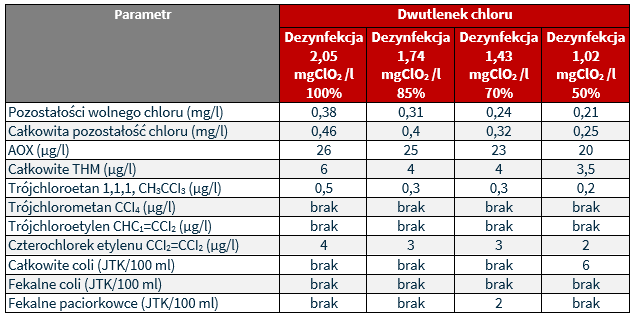
Porównując wyniki wody w zakresie dezynfekcji końcowej uzyskane z zastosowaniem podchlorynu sodu i dwutlenku chloru, można sformułować następujące wnioski:
- po dezynfekcji podchlorynem występuje podwyższone tworzenie się AOX, o wartościach znacznie przekraczających wartości dopuszczalne;
- dezynfekcja dwutlenkiem chloru jest skuteczniejsza niż podchlorynem sodu, ponieważ efektywniej redukuje parametry mikrobiologiczne, a jednocześnie nie tworzy ponadnormatywnych ubocznych produktów dezynfekcji.
- w analizowanym przypadku dawki dwutlenku chloru, powinny wynosić: około 1,5 mg ClO2/l w czasie wstępnego utleniania i 0,4 mg ClO2/l dla dezynfekcji końcowej.
Dwutlenek chloru w procesie dezynfekcji wody powierzchniowej (rzecznej) – pobierz pdf,
Dwutlenek chloru może być stosowany w uzdatnianiu wody pitnej jako środek dezynfekujący, albo jako utleniacz. Jako środek dezynfekujący może być stosowany zarówno w fazie wstępnej, jak i w fazie końcowej.
W dezynfekcji końcowej dwutlenek chloru ma podwójne działanie: bakteriobójcze i wirusobójcze w postaci CIO2 oraz bakteriobójcze i słabo bakteriobójcze w postaci chlorynu (CIO2–). Jako środek bakteriobójczy może pozostać aktywny w wodzie przez co najmniej 48 godzin, a jego skuteczność jest gwarantowana przez znacznie dłuższy czas niż chloru czy podchlorynu sodu W ten sposób zastosowanie dwutlenku chloru w tej fazie może gwarantować zahamowanie powtórnego wzrostu bakterii przy wtórnym skażeniu w sieci wodociągowej. Ponadto w odniesieniu do potencjalnego skażenia wirusowego, wirusobójcze i sporobójcze właściwości dwutlenku chloru są znacznie lepsze niż chloru czy podchlorynu sodu. Przy dezynfekcji końcowej stosuje się dawkę na poziomie 0,20 ÷ 0,40 mgCIO2/l, ponieważ nie powoduje ona przekroczenia ponadnormatywnych wartości sumy chlorynów i chloranów. Wartości te są ściśle związane z charakterem sieci wodociągowej, która w niektórych przypadkach może wymagać dalszego dochlorowania.
Dwutlenek chloru w dezynfekcji końcowej wody – pobierz pdf.,
Dwutlenek chloru w odniesieniu do dezynfekcji zbiorników wody pitnej odznacza się znacznie lepszymi właściwościami w porównaniu do podchlorynu sodu czy chloru gazowego. W przypadku zbiorników retencyjnych istotne jest określenie wymaganej dawki dezynfektanta uwzględniającą jakość retencjonowanej wody oraz teoretyczny czas przetrzymania wody w zbiorniku. W tym celu wykonano badania wody, których celem było znalezienie optymalnej dawki CIO2 w odniesieniu do chemicznych i mikrobiologicznych parametrów wody związanych z procesem dezynfekcji. Badania przeprowadzona dla dwutlenku chloru oraz podchlorynu sodu (chloru). Badań nie przeprowadzano dla ozonu z uwagi na jego krótkotrwały okres skuteczności (do 15 minut) w odniesieniu do zmiennego i długotrwałego okres retencji wody (nawet do 48 godzin) w połączeniu z typowym brakiem jednolitego czasu przetrzymania wody (tworzenie się tzw. kanałów dystrybucyjnych i zastoisk wodnych (martwe strefy)). Badaniom poddano trzy różne dawki dwutlenku chloru, w odniesieniu do procentowego zapotrzebowania i po 15-minutowym czasie kontaktu. Wyniki porównano z 1 mg chloru / podchlorynu sodu.
Odpowiednie dane zawarto w poniższej tabeli:
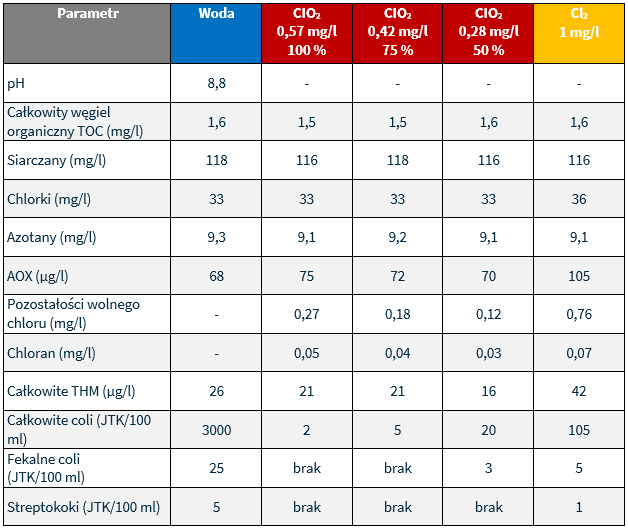
Godne uwagi jest to, że wartości AOX znacznie wzrosły (wzrost o 55 %) po dezynfekcji chlorem / podchlorynem sodu, podczas gdy po dezynfekcji dwutlenkiem chloru zawartość AOX wzrosła jedynie o 10 %. Podobne tendencje zaobserwowano również w odniesieniu do THMów.
Dwutlenek chloru w procesie dezynfekcji zbiorników – pobierz pdf,
Główne zastosowania dwutlenku chloru w tej dziedzinie to:
- dezynfekcja ścieków przed odprowadzeniem ścieków lub skierowaniem do recyklingu wody,
- usuwanie zapachów powstających w warunkach beztlenowych,
- poprawa szybkości sedymentacji osadu w procesach osadu czynnego,
- usuwanie zanieczyszczeń, takich jak czteroetylek ołowiu, cyjanki, azotyny, siarczki, węglowodory aromatyczne, fenole i tym podobne.
Dezynfekcja ścieków jest etapem procesu oczyszczania, który będzie nabierał coraz większego znaczenia, zwłaszcza w przypadku ponownego wykorzystania oczyszczanych ścieków. Tradycyjne procesy oczyszczania ścieków nie zapewniają całkowitej eliminacji ryzyka skażenia mikrobiologicznego wód zasilanych przez odpływające z oczyszczalni ścieki.
W przypadku zrzutów ścieków do wód w pobliżu kąpielisk, rozporządzenie Wspólnoty Europejskiej (Dyrektywa WE nr 76/169) przewiduje maksymalnie 2000 kolonii bakterii coli na 100 ml i odpowiedni 100 jednostek kałowych bakterii coli również na 100 ml. W przypadku metody opartej na chlorze i podchlorynie sodu obecność w ściekach znacznych ilości amoniaku i substancji organicznych powoduje znaczące zużycie środka dezynfekującego z jednoczesnym tworzeniem się chloramin (które to mają 80 razy mniejsze działanie bakteriobójcze w porównaniu z wolnym chlorem). Ponadto, w wyniku reakcji z substancjami organicznymi, chlor i podchloryn sodu wytwarzają chlorowcowe związki organiczne (AOX), które mogą kumulować się w środowisku i zanieczyszczać wody. Taka sytuacja może skutkować bardzo istotnymi konsekwencjami w przypadkach, gdy oczyszczona woda zostanie ponownie wykorzystana do celów nawadniania. Dwutlenek chloru nie wchodzi w reakcję z amoniakiem, tworzy ograniczone ilości chlorowcopochodnych związków organicznych w obecności substancji organicznych, utlenia fenole i jest aktywny w szerokim zakresie pH. Tworzy wymienną pozostałość, która może być użyta do automatycznego dozowania, i zazwyczaj nie wymaga kolejnej fazy odchlorowania (np. z wodorosiarczynem sodu).
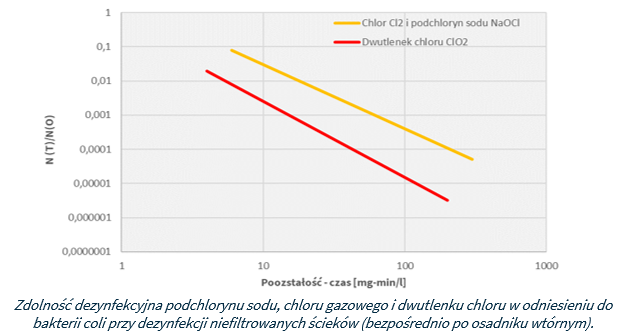
Badania przeprowadzone przez Amerykańską Agencję Ochrony Środowiska (US-EPA) na ściekach po osadnikach wtórnych (filtrowanych i niefiltrowanych na trzecim stopniu) wykazały, że po 60 minutowym czasie kontaktu, do osiągnięcia takiego samego stopnia unicestwienia wszystkich bakterii z grupy coli dawki dwutlenku chloru są od 2 do 70 razy mniejsze niż w przypadku chloru czy podchlorynu sodu.
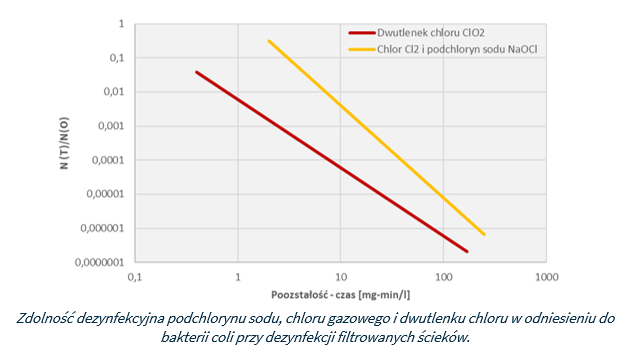
Ponadto testy laboratoryjne przeprowadzone przez amerykańską Agencję Ochrony Środowiska (US-EPA) na ściekach komunalnych wykazują, że dezynfekowane za pomocą dwutlenku chloru ścieki nie zawierają mierzalnych ilości trójchlorometanów a chlorowanych związków organicznych jest od 10 do 20 razy mniej w porównaniu z tą samą dawką chloru czy podchlorynu sodu.
Bakteriobójcza i wirusobójcza skuteczność dwutlenku chloru rekomenduje go przy dezynfekcji ścieków szpitalnych. Badania laboratoryjne przeprowadzone na próbkach ścieków pochodzących z oddziału chorób zakaźnych szpitala miejskiego, potwierdzają bardzo wysoką skuteczność dwutlenku chloru, przy jednoczesnym występowaniu bardzo niewielkich formacji chlorowcowanych organicznych produktów ubocznych (AOX).Aktywność wirusobójczą oceniano poprzez skażenie nieoczyszczonych ścieków szczepionką poliowirusową typu 1 (wiremia 200 000 TCID50) i poddawanie jej działaniu coraz większych dawek dwutlenku chloru (5, 10 i 15 mg/l) przez 30 minut. Wysoki odsetek dezaktywacji wirusa odnotowano już przy dawce 5 mgCIO2/l a całkowite unicestwienie miało miejsce przy dawce 10 mgCIO2/I. Ze względu na dużą zmienność chemiczną i biologiczną ścieków oraz różne możliwości oczyszczania, którym mogą być poddawane ścieki, dawka dwutlenku chloru może się znacznie różnić. Do podstawowych parametrów różnicujących dawkę należy: zawiesina ciał stałych, zawartości bakterii, zawartości węgla organicznego, temperatury i pH. W ściekach, które zostały poddane procesowi oczyszczania trzeciego stopnia i mają zawartość rozpuszczonego węgla organicznego i zawiesiny poniżej 10 mg/l, przy odpowiednim mieszaniu, konieczna jest na ogół dawka na poziomie 1,5 – 2,0 mgCIO2/l przy czasie kontaktu nawet krótszym niż 15 minut. W tych warunkach dawka operacyjna stanowi około 20-30% całkowitego zapotrzebowania na CIO2. W przypadku ścieków szpitalnych, które mogą zawierać dużą ilość mikroorganizmów odpowiedzialnych za poważne infekcje, dawka powinna wynosić ok. 10 mgClO2/l.
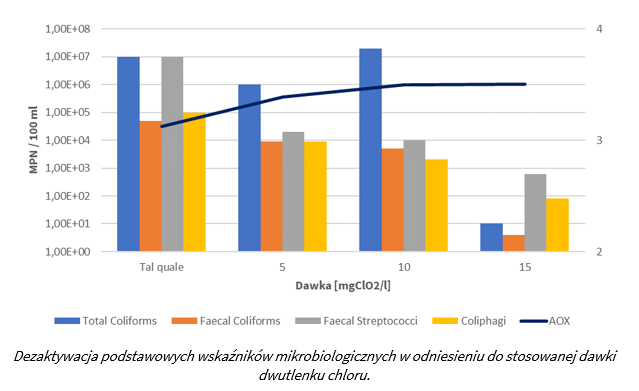
Dezynfekcja ścieków szpitalnych dwutlenkiem chloru – pobierz pdf,
Dwutlenek chloru jest z powodzeniem wykorzystywany w wielu zastosowaniach w przemyśle spożywczym, a w szczególności w następujących obszarach działalności i operacjach:
- mycie i transport owoców i warzyw oraz przetwarzanie ryb i mięsa;
- dezynfekcja wód chłodzących;
- mycie pojemników na żywność i napoje;
- produkcja żywności mrożonej;
- produkcja piwa.
Mycie i transport owoców i warzyw oraz produkcja mięsa
W procesie przechowywania i przetwarzania owoców i warzyw produkty są transportowane z punktu rozładunku do zakładu przetwórczego za pomocą strumienia wody. Dwutlenek chloru jest dozowany do wody w transportowej, aby kontrolować mikroorganizmy obecne na powierzchni produktów, zredukować potencjalne skażenie w zakładzie oraz w celu ograniczenia czasu i kosztów związanych z czyszczeniem kanałów transportowych. Obróbka wody transportowej z użyciem dwutlenku chloru zamiast chloru czy podchlorynu sodu ma tę zaletę, że nie tworzy chloramin lub innych niepożądanych produktów ubocznych, które mogą być niebezpieczne dla zdrowia ludzkiego. Ponadto chloroaminy mogą powodować zmiany organoleptyczne w produkcie (nieprzyjemne smaki i zapachy).
Dla tego typu zastosowania, dawka CIO2 w dużym stopniu zależy od rodzaju żywności i związanego z nią poziomu mikrobiologicznego zanieczyszczenia. Na ogół waha się ona od 2 ppm (w celu zapewnienia resztkowego dwutlenek chloru na poziomie około 0,5 ppm) do 5 ppm np. dla przetwórstwa krewetek i do 9 ppm dla przetwórstwa kurczaków. Przy zdecydowanie wyższej dawce, dwutlenek chloru może być stosowany również do uzdatniania wody używanej do mycia, transportu, przetwarzania i sortowania świeżych produktów przed ich sprzedażą (100 – 150 mgClO2/l) oraz do wstępnej regeneracji (200 – 250 mgClO2/l), która ma na celu spowolnienie procesów dojrzewania/przerastania i rozwoju patogenów (zwłaszcza grzybów).
Dezynfekcja wód chłodzących
Zadowalające wyniki uzyskano także przy zastosowaniu dwutlenku chloru do dezynfekcji wody chłodzącej do pojemników na żywność. W rzeczywistości ważne jest, aby woda ta była używana bez mikroorganizmów w celu uniknięcia możliwych dalszych skażeń bakteryjnych w żywności, a w konsekwencji pogorszenia jakości produktu oraz możliwego zatrucia mikrobiologicznego i/lub infekcji.
Co więcej, użyteczne w tym przypadku jest używanie wody chłodzącej wolnej od drobnoustrojów. Dla tego zastosowania zaleca się dawkę 1,2 -1,5 ppm dwutlenku chloru lub taką, która pozostawi w każdym przypadku pozostałość pomiędzy 0,2 a 0,5 ppm.
Mycie pojemników na żywność i napoje
Na jakość produktu spożywczego (płynnego lub stałego) może mieć wpływ niewłaściwe mycie i dezynfekcja pojemników, w których dany produkt będzie przechowywany. Mycie pojemników jest szczególnie ważne w przypadkach, gdy mają one zawierać produkty, które łatwo ulegają biodegradacji (takie jak mleko, piwo, soki owocowe i napoje bezalkoholowe). Na przykład w procesie mycia szklanych butelek zapewnia się drugie płukanie, które odbywa się w warunkach idealnych dla rozwoju bakterii (temperatura około 30 – 40°C, wysoka wilgotność i pH około 9). Z tego powodu należy zapewnić kontrolę mikrobiologiczną poprzez zastosowanie dezynfekcji opakowań. Dezynfekcja dwutlenkiem chloru jest lepsza niż dezynfekcja podchlorynem, ponieważ dwutlenek chloru jest nadal aktywny przy wysokim pH i nie tworzy chlorofenoli ani związków organicznych o działaniu halogenowym. Pojemniki są dezynfekowane za pomocą dwutlenku chloru o stężeniu od 0,5 do 2 ppm, w zależności od właściwości wody, ale w każdym przypadku ważne jest, aby mieć około 0,2 ppm jego pozostałość. Przy dezynfekcji dwutlenkiem chloru wystarczy bardzo krótki czas kontaktu (nawet krótszy niż jedna minuta).
Produkcja żywności mrożonej
Oprócz oczyszczania wody używanej do transportu i mycia, dwutlenek chloru może być używany w procesie produkcji mrożonej żywności do dezynfekcji wody używanej np. do zamrażania. Proces ten jest stosowany przetworzeniu produktu finalnego (np. mycie, krojenie w plastry, siekanie itp.). W rzeczywistości, jeśli dany obieg wody nie jest poddawany dezynfekcji, może dojść do zanieczyszczenia mikrobiologicznego, najczęściej przez bakterie typu Listeria, ponieważ przetrwają one nawet w niskich temperaturach. Aby uniknąć tego problemu, woda w zamrażalniku jest dezynfekowana dwutlenkiem chloru w taki sposób, aby zapewnić 0,2 – 0,5 ppm jego pozostałości.
Produkcja piwa
Piwowarstwo potrzebuje 6 – 10 litrów wody na litr wyprodukowanego piwa. Woda wchodząca w skład produktu końcowego musi być oczywiście wolna od mikroorganizmów i nie może nadawać piwu żadnych zapachów ani smaków zmieniających jego smak. Obróbka na bazie dwutlenku chloru i w tym przypadku ma kilka zalet, ponieważ nie produkuje chlorofenoli i tylko znikomą ilość chlorowanych związków organicznych, ponadto nie wpływa na smak piwa i gwarantuje eliminację mikroorganizmów nawet w dużym zakresie pH (6÷9). Dla tego zastosowania dawka może wahać się od 0,05 do 0,5 ppm.
W przemyśle spożywczym możliwe jest zintegrowane zastosowanie dwutlenku chloru, jak również jego konwekcja we wszystkich operacjach, w których wykorzystywana jest woda.
- woda zasilająca (woda pierwotna) i/lub przeznaczona do spożycia przez ludzi (w przypadku, gdy jest pobierana ze studni i nie jest dystrybuowana przez system wodociągowy);
- woda do ogólnego mycia (woda do mycia lub transportu);
- woda chłodząca (w przemyśle konserwowania pomidorów (parowniki, wieże), w browarach, w fabrykach serów i mleczarniach, w przemyśle przetwórstwa mięsa gotowanego, w fabrykach konserw, gdzie żywność jest konserwowana po sterylizacji termicznej);
- woda używana do przetwarzania (na przykład w browarach, przetwórstwie krewetek oraz kurczaków);
- ścieki (przy dezynfekcji przed ich odprowadzeniem do środowiska).
Dezynfekcja dwutlenkiem chloru w przemyśle spożywczym – pobierz pdf,
Złożone osady zanieczyszczeń, które mogą zawierać mikro i makrobiologiczne substancje, cząstki nieorganiczne i produkty korozji, stanowią istotny problem w odniesieniu do wydajności systemów wody chłodzącej, wymienników ciepła i systemów rurociągów. Pierwszym etapem powstawania zanieczyszczeń jest niekontrolowany wzrost mikroorganizmów na powierzchniach, ze wstępnym utworzeniem biofilmu w wyniku procesów życiowych żywych komórek i ich pozostałości metabolicznych czego efektem jest powstający śluz.
Mechanizm powstawania biofilmu (błony pochodzenia biologicznego) można podsumować w następujący sposób:
- powierzchnie pokrywane są pierwotnymi bakteriami kolonizującymi i innymi organizmami;
- w etapie przejściowym rozwijają się wielowarstwowe komórki, osadzające się w swoim materiale polimerowym;
- w etapie końcowym gęstość populacji szybko wzrasta, co prowadzi do powstawania biofilmu.
Biofilm jest substratem prowadzącym do osadzania się i przylegania innych materiałów biologicznych i nieorganicznych. Jednakże termin „obrastanie” jest używany w odniesieniu do końcowej mieszaniny biofilmu, zawiesiny ciał stałych, produktów korozji i makroorganizmów, które następnie przylegają i rosną na powierzchniach. Obrastanie osiąga maksymalny rozwój po przylgnięciu organizmów morskich lub pochodzących z morza. Ogólnie rzecz ujmując rozróżniamy makro i mikro obrastanie. Makro-obrastanie odnosi się do wzrostu skorupiaków (Barnacles), mięczaków (Mussels i Clams) oraz koelenteratów (Hydroids), podczas gdy mikro-obrastanie dotyczy glonów i bakterii.
Obrastanie jest szkodliwe i powoduje:
- wyższe koszty eksploatacji, ponieważ mniejsza wymiana ciepła powoduje straty produkcyjne, a wzrost oporów przepływu wymaga większej ilości energii do pompowania;
- wyższe koszty konserwacji, w przypadku operacji czyszczenia lub wymiany uszkodzonych rur na skutek korozji pod obrostami lub przegrzania,
- krótszy czas pracy, ponieważ konieczne są dłuższe przestoje w celu oczyszczenia lub naprawy urządzeń.
W procesie obrastania istotne są również następujące parametry wody:
- temperatura – tempo wzrostu drobnoustrojów zależy od sezonowych wahań temperatury;
- rozpuszczony gaz – zawartość tlenu wpływa na wzrost wielu gatunków organizmów wodnych;
- dostępność składników pokarmowych (fosfor i azot) – są to podstawowe elementy niezbędne do biosyntezy;
- pH i zawiesiny ciał stałych.
Wzrostowi bio-obrastania można częściowo zapobiec w fazie projektowania, stosując odpowiednie materiały (np. miedź, stal nierdzewną AISI 316 lub obróbkę powierzchni specjalnymi polimerami) oraz poprzez wymiarowanie rur w taki sposób, aby uzyskać prędkość przepływu powyżej 1 m/s, która to będzie utrudniała przyleganie organizmów. Ponadto istnieją fizyczne i chemiczne metody zapobiegania obrastaniu w instalacjach wody chłodzącej. Zabiegi fizyczne są stosowane głównie podczas przestojów. Oczyszczanie chemiczne opiera się na nieutleniających biocydach lub na utleniających biocydach, takich jak np. chlor gazowy, podchloryn sodu czy dwutlenek chloru. Zgodność z przepisami dotyczącymi jakości odprowadzanej wody oraz konieczność stosowania bezpiecznych biocydów, doprowadziła do wyboru dwutlenku chloru jako biocydu do systemów chłodzenia w dużych zakładach. Podchloryn sodu lub chlor są jak najbardziej skuteczne w zwalczaniu obrastania przy wodach o wysokiej zawartości substancji organicznych, jednakże prowadzą one do powstawania chlorowcowanych związków organicznych (w szczególności trójchlorometanów), które są uwalniane do środowiska. Czasami ilość chloru lub podchlorynu wymagana do utrzymania systemu w czystości jest tak duża, że wymaga użycia dodatkowego środka redukującego (w celu obniżenia wartości chloru resztkowego przy zrzucie). Taka sytuacja ma zdecydowanie mniejszy wymiar przy stosowaniu dwutlenku chloru.
Przypadek 1
W hucie stali pobierane jest 120’000 m3/h eutroficznej wody morskiej z obszaru o ograniczonej wymianie wody z otwartym morzem. Po wykorzystaniu woda jest odprowadzana do innego, większego zbiornika morskiego, gdzie hodowane są omułki. Woda wejściowa jest biologicznie wysoko zanieczyszczona. Ma pH w zakresie 8,1 – 8,4 przy średniej temperaturze 27°C w lecie i 15°C w zimie. Do określania wskaźnika bio-obrastania stosowane są systematyczne pomiary, z których wynika, że średnia wartość obrostu wynosi 65 kg/m2 rocznie, ale wiosną i latem wartość ta osiąga 10-15 kg/m2 miesięcznie. Zapotrzebowanie wody zasilającej na CIO2 wynosi od 1,2 do 1,8 mg/l. Po rozpoczęciu testów zastosowano ciągłe dawkowanie CIO2 na poziomie 0,5 ppm, przy starannym monitorowaniu biomasy i kontroli wizualnej przez kamery i nurków. Dozowanie dwutlenku chloru ograniczyło przyrost biomasy w takim stopniu ze dawkowanie mogło być zmniejszone do 0,5 mgClO2/l przez 10 godzin dziennie w czasie zimowym i 14 godzin dziennie w czasie letnim. Zabieg ten poza tym, że jest skuteczny, okazał się być przyjazny dla materiałów i środowiska.
Przypadek 2
Dwutlenek chloru został użyty do kontroli rozwoju makro-obrostów (równowartość 25 kg/m2 rocznie) w wodzie chłodzącej jednej z elektrowni o mocy 1 260 MWe. Elektrownia ta potrzebuje 120’000 m3/h wody morskiej. Dezynfekcje wody dwutlenkiem chloru stosowano w sposób ciągły w dawkach od 0,1 do 0,2 mgClO2/l CIO2, co odpowiada średnio 0,13 mgClO2/l rocznie. W zakładzie tym, przeprowadzono eksperymenty w celu uzyskania przybliżonych wskazań do stosowania dawek CIO2. Wzrost gatunków odpowiedzialnych za obrastanie został zahamowany przez ciągłe dawkowanie 0,07 ppm CIO2 w miesiącach zimowych (grudzień – kwiecień) i 0,18 ppm w miesiącach letnich (maj – listopad). W związku ze słabym tworzeniem się produktów ubocznych degradacji CIO2, które były pod kontrolą we wszystkich fazach doświadczenia, dwutlenek chloru okazał się najskuteczniejszy w zwalczaniu tych zanieczyszczeń.
Obróbka wody chłodzącej dwutlenkiem chloru, biofilm – pobierz pdf.
Dwutlenek chloru może być wytwarzany w generatorach, bezpośrednio w miejscu jego dozowania. Proces produkcji dezynfekanta nie jest skomplikowany i polega na proporcjonalnym mieszaniu roztworów chlorynu sodowego (7,5%) oraz kwasu solnego (9%). Proces ten jest najczęściej stosowany w branży uzdatniania wody ze względu na niezawodność działania oraz dostępność produktów, z których jest produkowany dwutlenek chloru. Spełnia on najbardziej zróżnicowane wymagania w zakresie użytkowania, bezpieczeństwa, niezawodności i łatwości dozowania do wody.
Przygotowanie dwutlenku chloru odbywa się poprzez zakwaszenie chlorynu w następującej reakcji:
5 ClO2– + 4 H3O+ → 4 ClO2 + Cl + 6 H2O
Wprowadzanie jonu Cl– do systemu za pomocą kwasu solnego jest łatwiejsze niż w przypadku innych kwasów. Najczęstszą metodą produkcji dwutlenku chloru jest użycie chlorynu sodu i kwasu solnego w następującej reakcji:
5 NaClO2 + 4 HCl → 4 ClO2 + 5 NaCl + 2 H2O
Otrzymany roztwór dwutlenku chloru może zatem zawierać chlor i chlorany, oprócz oczekiwanych chlorków. Odpowiednie warunki pracy umożliwiają produkcję roztworów CIO2 bez Cl i w małych ilościach (mniej niż 5 %) CIO3–.
Przy spełnieniu odpowiednich warunków możliwe jest uzyskanie wysokiej wydajności produkowanego dwutlenku chloru (zbliżonym do teoretycznego – 4 mole CIO2 na 5 moli NaCIO2). Do głównych tych czynników należy:
- zastosowanie nadmiaru HCI, co w praktyce oznacza użycie prawie takiej samej ilości wagowej chlorynu sodu i kwasu solnego (kwas solny w ilości przekraczającej 300% w stosunku do ilości stechiometrycznej);
- maksymalne obniżenie stężenia ClO2 w wyprodukowanym roztworze;
- kontrolę pH, które musi być utrzymywane poniżej 0,5 (przy pH = 1 reakcja jest bardzo powolna, a chloryn jest tylko częściowo przekształcany);
- używanie zmiękczonej wody do rozcieńczania chlorynu (unikanie wytrącania się węglanów, które spowalniają reakcję);
- zapewnienie odpowiedniego mieszania, które jest niezbędne dla uzyskania dobrej wydajności produkcji.
Ponadto na szybkość reakcji produkcji dwutlenku chloru ma wpływ także temperatura. W przypadku produkcji CIO2 w niskich stężeniach szybkość reakcji może ulec znacznemu obniżeniu (nawet o współczynnik 3), jeśli temperatura układu zostanie obniżona z 20°C do 10°C.
Wytwarzanie dwutlenku chloru z chlorynu sodu i kwasu solnego – pobierz pdf.
Proces generowania dwutlenku chloru rozpoczyna się od zmieszania roztworów chlorynu sodu i kwasu solnego o dwóch różnych poziomach stężenia. Wybór stężenia odczynników, które mają być użyte, jest funkcją wymaganej wydajności godzinowej. Rozcieńczone odczynniki, są zwykle używane do uzyskania wydajności mniejszej niż 400 gCIO2/h, natomiast stężone odczynniki są używane do uzyskania wyższej wydajności (stosowanie rozcieńczonych odczynników wymagałoby ich większych ilości i wiązałoby się z wysokimi kosztami magazynowania i transportu). W przypadku odczynników stężonych stosowane są roztwory 25% chlorynu sodu i 33% kwasu solnego, natomiast w przypadku odczynników rozcieńczonych stosowane są roztwory 7,5% chlorynu sodu i 9% kwasu solnego. Należy pamiętać, że stężenie odczynników w fazie reakcji (produkcji) jest w obu przypadkach takie samo, ponieważ za każdym razem, gdy używane są odczynniki stężone, generator jest wyposażony w urządzenie przeznaczone do ich rozcieńczania.
Z uwagi na większa powszechność stosowania metody rozcieńczonej poniższy opis działania będzie się odnosił do tego typu generatorów. Optymalny proces produkcji odbywa się przy spełnieniu następujących warunków technicznych:
- generowanie dwutlenku chloru odbywa się wewnątrz komory reakcyjnej, zaprojektowanej tak, aby wytrzymać ciśnienie 10 barów, o objętości wystarczającej zapewniającej minimum 10 minutowy czasu reakcji;
- odczynniki są zasysane przez niezależne pompki dozujące;
- roztwór dwutlenku chloru wydostający się z komory reakcji o stężeniu około 20 g/l jest następnie rozcieńczany do stężenia poniżej 2 g/l przez dodatkowy przepływ wody. Proces rozcieńczania wyprodukowanego dwutlenku chloru może się odbywać zarówno w komorze jak i poza nią;
- ilość produkowanego dwutlenku chloru zależy od ilości odczynników użytych w procesie, a więc od częstotliwości pulsacji pompy;
- częstotliwość lub wydajność procesu produkcji dwutlenku chloru zależy od poziomu w zbiorniku wyprodukowanego roztworu ClO2 lub sygnału pochodzącego z przepływomierza (układ na sztywno o niewielkich różnicach wydajnościowych spowodowanych wymaganym czasem reakcji);
- generatory musza być wyposażone w systemy wykrywania zakłóceń eksploatacyjnych, które wyłączają produkcję dwutlenku chloru, gdy nie są spełnione warunki bezpieczeństwa;
- Generatory powinny być bezwzględnie wyposażone w przepływomierze a nie czujniki przepływu. Czujnik przepływu zapewnia jedynie obecność przepływu a nie wielkość jego natężenia.
System „pompowy” jest często stosowany w generatorach małej i średniej wielkości, gdzie zastosowanie pomp dozujących zapewnia bardziej precyzyjny pomiar. System ten jest bardziej stabilny w czasie i jest mniej podatny na wahania temperatury oraz na zanieczyszczenia stałe, które mogą być obecne w odczynnikach. Zmiany temperatury odczynników determinują zmiany ich gęstości i lepkości. Biorąc pod uwagę fakt, że dozowanie odbywa się w stałej objętości, przy produkcji ClO2 mogą występować zmiany w wydajności z uwagi na fakt, że na wskazanie przepływomierza wpływa temperatura. Błąd wskazania dla zmiany temperatury o 10°C wynosi ok. 7,5% (przepływomierze są zwykle kalibrowane w temperaturze 20°C). Zmiany te mogą być korygowane przez ręczne zmiany nastawów.
Generatory dwutlenku chloru – główne parametry – pobierz pdf.
Kwas solny jest cieczą parującą, gdy występuje w stężeniach powyżej 20% objętości. Jest to silny kwas, który atakuje większość metali z uwalnianiem wodoru. Oprócz indywidualnej ochrony osób zajmujących się jego obsługą – odpowiednich rękawic, obuwia i masek – należy zapewnić prysznic do mycia w przypadku rozlania lub przepełnienia w pobliżu zbiornika magazynowego.
Kwas solny, dostarczany luzem, jest zazwyczaj odprowadzany za pomocą pompy odśrodkowej wykonanej z tworzywa sztucznego z prostym mechanizmem zewnętrznym lub magnesem wahadłowym. Szczególną uwagę należy zwrócić na zabezpieczenie pompy przed pracą „na sucho” (poziomowskazy, ciśnieniomierze i amperometry z kontaktem minimalnego poziomu) oraz przed pracą z zamkniętym wylotem. Rury do kwasu solnego mogą być wykonane z tworzywa sztucznego, tak samo jak i zawory. Preferowane jest, aby rury krytyczne pod ciśnieniem lub zagrożone uderzeniem, jak również rury łączące, były wykonane z tworzywa sztucznego wzmocnionego włóknem szklanym, lub lepiej, ze stali wyłożonej tworzywem sztucznym.
HCl dodany do chlorynu sodu w stężonym roztworze powoduje natychmiastowe uwolnienie dwutlenku chloru, który w przypadku braku odpowietrzenia może spowodować awarię zbiornika. Ryzyko wystąpienia takich wypadków jest zazwyczaj związane z niewłaściwą wymianą króćców w zbiornikach magazynowych podczas rozładunku odczynników. W związku z tym zaleca się stosowanie korców o dwóch różnych średnicach do rozładunku oraz urządzeń kontrolnych, takich jak pH-metr z alarmem, który wyłącza pompę tłoczącą.
Zbiorniki magazynowe mogą być wykonane z poliestru bisfenolowego lub winylowego typu (PRFV), który jest materiałem starzejącym się i powinny być wymieniane co 10 lat.
W przypadku małych magazynów z lepszymi rezultatami można zastosować polietylen (PE), natomiast w przypadku dużych zbiorników o pojemności powyżej 20 m3 zaleca się stosowanie PVC wzmocnione poliestrem (PVC + PRFV) i stalą wyłożoną gumą. Zbiornik magazynowy musi być wyposażony w rurę przelewową, która pełni również funkcję odpowietrznika oraz miernika poziomu, aby bezpiecznie obsługiwać operacje napełniania. Gaz nasycony HCI musi być najpierw wypłukany przed rozładunkiem.
Zbiornik HCl musi być umieszczony w zbiorniku ochronnym o objętości równej objętości samego zbiornika plus 10 % i wyłożonym materiałem kwasoodpornym (bitumem na bazie gumy, płytkami lub poliestrem).
Produkt ten jest zwykle sprzedawany w postaci roztworu wodnego w postaci jasnożółtej i klarownej cieczy o lekkim zapachu chloru. Przy mniejszych ilościach chloryn sodu może być w postaci stałej w formie białych kryształków. Stały chloryn sodu jest utleniaczem i dlatego nie może wchodzić w kontakt z materiałami organicznymi łatwopalnymi takimi jak: guma, papier, słoma lub drewno. Po zmieszaniu chlorynu sodu z kwasami powstaje CIO2, dlatego należy mieć na uwadze wymagane aspekty dotyczące bezpieczeństwa stosowania i składowania. Ze względów bezpieczeństwa zaleca się stosowanie roztworów chlorynu sodu zamiast jego formy stałej. Roztwór chlorynu sodu jest łatwiejszy w użyciu, nie wydzielają drażniących pyłów oraz jest pozbawiony ryzyka błędów w przygotowaniu do użycia. Ponadto, roztwory chlorynu nie są klasyfikowane jako „utleniacze”. Z drugiej strony, takie roztwory mogą krystalizować się w niskich temperaturach np. poniżej -3°C.
Materiały, które są zgodne z chlorynem sodu w roztworze to: PVC, polietylen, poliester bisfenolowy, winyloester, stal nierdzewna AISI 316 lub lepiej 316L, ponieważ chloryn może powodować korozję w miejscach spawów.
Zbiorniki magazynowe mogą być wykonane ze wszystkich powyższych materiałów z zaznaczeniem, że w przypadku dużych zbiorników bardziej ekonomiczne jest zastosowanie poliestru bisfenolowego, malowanego zewnętrznie, aby uniknąć pogorszenia jakości. Przy stosowaniu chlorynu sody należy bezwzględnie unikać kontaktu z żelazem, miedzią i jej stopami, aluminium oraz kauczukiem naturalnym lub syntetycznym. Właściwości konstrukcyjne tacy ochronnej i zbiornika magazynowego są takie same jak w przypadku kwasu solnego, z wyjątkiem wykładziny kwasoodpornej.
Należy pamiętać o wyposażeniu ochronnym tj. rękawice, gogle, odpowiednia odzież ochronna. Miejsca stosowania chlorynu sodu muszą być wyposażone w bieżącą wodę do natychmiastowego mycia w razie przypadkowego kontaktu z tym roztworem.
Dwutlenek chloru jest produkowany i stosowany w postaci roztworu wodnego. Problemy bezpieczeństwa są w rzeczywistości związane z właściwościami wybuchowymi dwutlenku chloru, gdy jego stężenie w powietrzu jest większe niż 10% objętości. Z tego powodu należy dołożyć wszelkich starań, aby zapobiec tworzeniu się jakichkolwiek kieszeni gazowych. Poniższy wykres przedstawia korelację pomiędzy stężeniem roztworu dwutlenku chloru a procentowym udziałem dwutlenku chloru w powietrzu w różnych temperaturach.
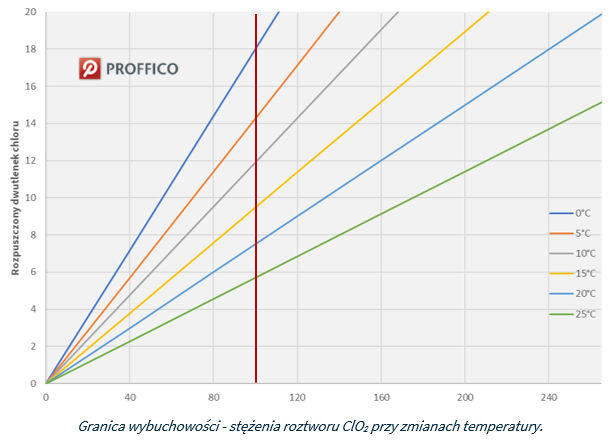
Dlatego ze względów bezpieczeństwa urządzenia generujące są zaprojektowane w taki sposób, aby mogły pracować w warunkach poniżej poziomu ryzyka. Stężenie CIO2 w roztworze na wyjściu z generatora nie może przekraczać 28 ÷ 30 g/l, oznacza to, że generatory wykorzystujące chloryn sodu i kwas solny, muszą być wyposażone w odpowiedni obwód rozcieńczający na wlocie reaktora, tak aby na wyjściu z generatora stężenie CIO2 nie przekraczało 20 g/l. Woda do rozcieńczania chlorynu sodu musi być zdemineralizowana lub zmiękczona, aby uniknąć wytrącania się węglanu wapnia. Wszystkie generatory muszą być wyposażone w przepływomierze do pomiaru odczynników i rozcieńczającej je wody. Urządzenia te muszą mieć możliwość wyłączenia pracy generatora w przypadku wystąpienia zakłóceń (np. braku jednego z odczynników).
Powstający w roztworze wodnym gaz o silnym zapachu podobnym do chloru może łatwo wyparować i jest wykrywalny w powietrzu w stężeniu od 1,4 do 1,7 ppm.
Stężenia CIO2 w powietrzu około 4,5 ppm mogą powodować podrażnienia dróg oddechowych, natomiast dłuższe ich wdychanie może powodować obrzęk płuc. Granica bezpieczeństwa ekspozycji w miejscu pracy wynosi 0,1 ppm. Urządzenia do generowania i dystrybucji dwutlenku chloru muszą być instalowane tylko w miejscach wyposażonych w odpowiednią wentylację. Dodatkowo zaleca się stosowanie analizatora zawartości ClO2 wykrywającego ponadnormatywną zawartość tego gazu w powietrzu.
Jako zabezpieczenie w przypadku wycieku w pobliżu generatora musi być dostępna maska wyposażona w filtr z węglem aktywnym do ochrony dróg oddechowych.
Materiały, które mają mieć kontakt ze stężonymi roztworami dwutlenku chloru, powinny być wykonane z teflonu, polifluorku winylidenu (PVDF) i polichlorku winylu (PVCu).
Dwutlenek chloru – bezpieczeństwo oraz przechowywanie – pobierz pdf.
Działanie utleniające dwutlenku chloru prowadzi do powstawania chlorynów, chlorków i małych ilości chloranów. Ilość wytworzonych chlorynów zwyczajowo osiąga wartość około 60-70% zużytego dwutlenku chloru, czyli 0,6 – 0,7 mg CIO2– na mg wykorzystanego CIO2. W odpowiednich warunkach stosowania dwutlenku chloru dominującą reakcją jest częściowa redukcja CIO2 do chloru, czyli pośredni etap redukcji dwutlenku chloru. Chlorany mogą powstawać w wyniku utleniania kwasu podchlorowego (HCIO) z chlorynu, co z kolei jest wynikiem reakcji CIO2 z niektórymi substancjami organicznymi, zgodnie z poniższą reakcją:
HClO + ClO2– + OH– → ClO3– + Cl– H2O
Ponadto niewielkie ilości kwasu podchlorowego w obecności substancji organicznych naturalnie występujących w wodzie (np. kwasy huminowe), powodują powstawanie bardzo małych ilości halogenków organicznych ogółem (Total Organic Halides – TOX). Obecność chloranów jest związana z wydajnością i sposobem produkcji dwutlenku chloru i potencjalną fotolizą po ekspozycji na światło słoneczne.
Dostępne obecnie badania toksykologiczne wskazują, że dawki dwutlenku chloru, chlorynów (CIO2–) i chloranów (CIO3–) stosowanych w uzdatnianiu wody nie stanowią żadnego zagrożenia dla zdrowia. Wyniki badań klinicznych i biochemicznych, przeprowadzonych w Stanach Zjednoczonych, dotyczących wpływu dwutlenku chloru spożywanego w drodze regularnego spożycia wody, wskazują, że próg stężenia chlorynów, powyżej którego może istnieć pewien wpływ na zdrowie, jest równy 24 ppm dla zdrowych osób fizycznych i 5 ppm dla osób dotkniętych niedoborem enzymu G6PD (dehydrogenazy glukozowo-6-fosforanowej). Badania toksykologiczne przeprowadzone na zwierzętach wykazały, że stężenie chlorynu, przy którym zaczyna pojawiać się stres hemolityczny, wynosi 250 ppm. W Polsce w rozporządzeniu Ministra Zdrowia „W sprawie jakości wody przeznaczonej do spożycia Przez ludzi” nie określono maksymalnego stężenia dwutlenku chloru w wodzie, określono natomiast maksymalna wartość sumy chlorynów i chloranów która wynosi odpowiednio 0,7 mg/l (mierzona w punkcie czerpnym u konsumenta).
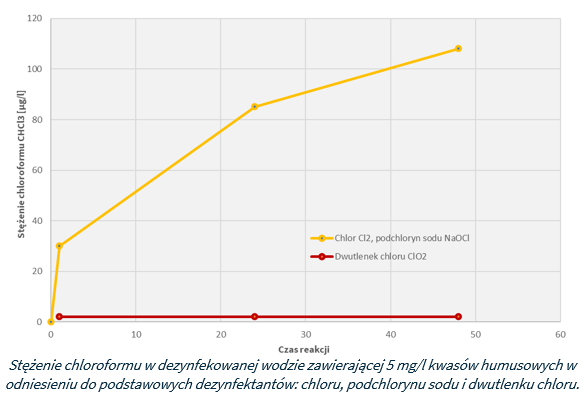
Przy dezynfekcji wody dwutlenkiem chloru należy zwrócić uwagę na potencjalne tworzenie się związków organicznych zawierających chlorowce jako uboczne produkty utleniania rozpuszczalnych frakcji organicznych (naturalna materia organiczna). W obecnym stanie techniki i wiedzy, trójhalometany (THM) stanowią skuteczny wskaźnik całkowitej zawartości chlorowcowanych związków organicznych i są powszechnie stosowane w ocenie procesu dezynfekcji (w odniesieniu do powstawania tego rodzaju produktów ubocznych). Zatem ocena THM jest logicznie uzasadniona, ponieważ stanowi ona frakcję potencjalnie najbardziej toksyczną dla zdrowia człowieka.
Porównanie wartości THMów dla chloru i dwutlenku chloru zawiera poniższa tabela: